
Annex 1 – First Air
5 Min. Lesezeit | von Michael Kuhn, Benjamin Pfändler
Erschienen im LOGFILE 06/2026
Mit dem überarbeiteten Annex 1 des EU-GMP-Leitfadens rückt der Schutz der sogenannten First Air stärker in den Fokus. Strömungshindernisse oder Eingriffe müssen daher im Rahmen der Contamination Control Strategy risikobasiert bewertet werden.
Der Anhang 1 zum GMP-Leitfaden ist im August 2022 neu erschienen. Die Strömungsvisualisierung und die Luftströmung haben seither eine sehr viel größere Bedeutung gewonnen und werden daher auch bei GMP-Inspektionen stärker in den Fokus gerückt. Die Hersteller steriler Arzneimittel und die Lieferanten des dafür erforderlichen Equipments, sind stark durch das Thema "First Air Protection" herausgefordert. Die Maschinen und Prozesse müssen dementsprechend optimiert werden. Da sich Luftverwirbelungen in Sterilbereichen der Klasse A nicht (vollständig) verhindern lassen, muss im Einzelfall bewertet werden, ob die First Air Protection dennoch gewährleistet ist.
Grundlagen [1]
Glossar
Erstluft: Bezieht sich auf gefilterte Luft, deren Strom vor dem Kontakt mit dem exponierten Produkt und den produktberührenden Oberflächen nicht unterbrochen wurde, wodurch die Luft vor dem Erreichen der kritischen Zone kontaminiert werden könnte.
Kritische Zone: Ein Ort innerhalb des aseptischen Verarbeitungsbereichs, an dem das Produkt und kritische Oberflächen der Umgebung ausgesetzt sind.
Kritische Oberflächen: Oberflächen, die direkt mit einem sterilen Produkt oder seinen Behältnissen oder Verschlüssen in Kontakt kommen oder diese direkt beeinflussen können. Kritische Oberflächen werden vor Beginn des Herstellungsvorgangs sterilisiert, und die Sterilität wird während der gesamten Verarbeitung aufrechterhalten.
Auszüge aus dem Annex 1 mit Anforderung First Air Protection
Klasse A: Die kritische Zone für Arbeitsvorgänge mit hohem Risiko (zum Beispiel aseptische Prozesslinie, Abfüllbereich, Stopfenbehälter, offene Primärverpackungen) oder zur Herstellung aseptischer Verbindungen unter dem Schutz der Zuluft direkt nach dem Filter (Erstluft) (...)
Isolatoren: Die Konstruktion offener Isolatoren sollte Bedingungen der Reinheitsklasse A mit Erstluftschutz in der kritischen Zone und einem unidirektionalen Luftstrom gewährleisten, der während der Verarbeitung über die exponierten Produkte hinwegströmt und von ihnen wegführt (...)
RABS: Die Auslegung von RABS sollte Bedingungen der Reinheitsklasse A mit unidirektionalem Luftstrom und Erstluftschutz in der kritischen Zone gewährleisten (...)
Risikobewertung: Bei der Durchführung der Risikobewertung für die CCS eines Isolators sollten unter anderem folgende Punkte berücksichtigt werden: (...) die Auswirkungen von Handschuhmanipulationen, die die Luftströmung oberhalb kritischer Prozesspunkte beeinträchtigen könnten (...)
RABS: Bewegung in der Nähe der kritischen Zone sollte eingeschränkt und eine Behinderung des unidirektionalen Luftstroms (Erstluft) vermieden werden. Eine Bewertung von Studien zur Visualisierung von Luftströmungen sollte als Teil des Schulungsprogramms in Betracht gezogen werden (...)
Erklärung des First Air-Prinzips anhand eines Beispiels
Anhand eines Beispiels soll das Prinzip der First Air erläutert werden. Abbildung 1 zeigt schematisch den Strömungsverlauf in einem Bereich der Reinheitsklasse A mit turbulenzarmer Verdrängungsströmung. Erstluft (First Air) ist die aus dem Filter austretende Luft, welche auf ihrem Weg nicht kontaminiert wird. Da es innerhalb der Luftströmung immer wieder Hindernisse gibt, die umströmt werden müssen, ist zu bewerten, ob dies zu einer potentiellen Kontamination führt. Im dargestellten Beispiel sind mehrere typische Störgrößen dargestellt, welche risikobasiert bewertet werden müssen (Teil der Contamination Control Strategy – CCS).
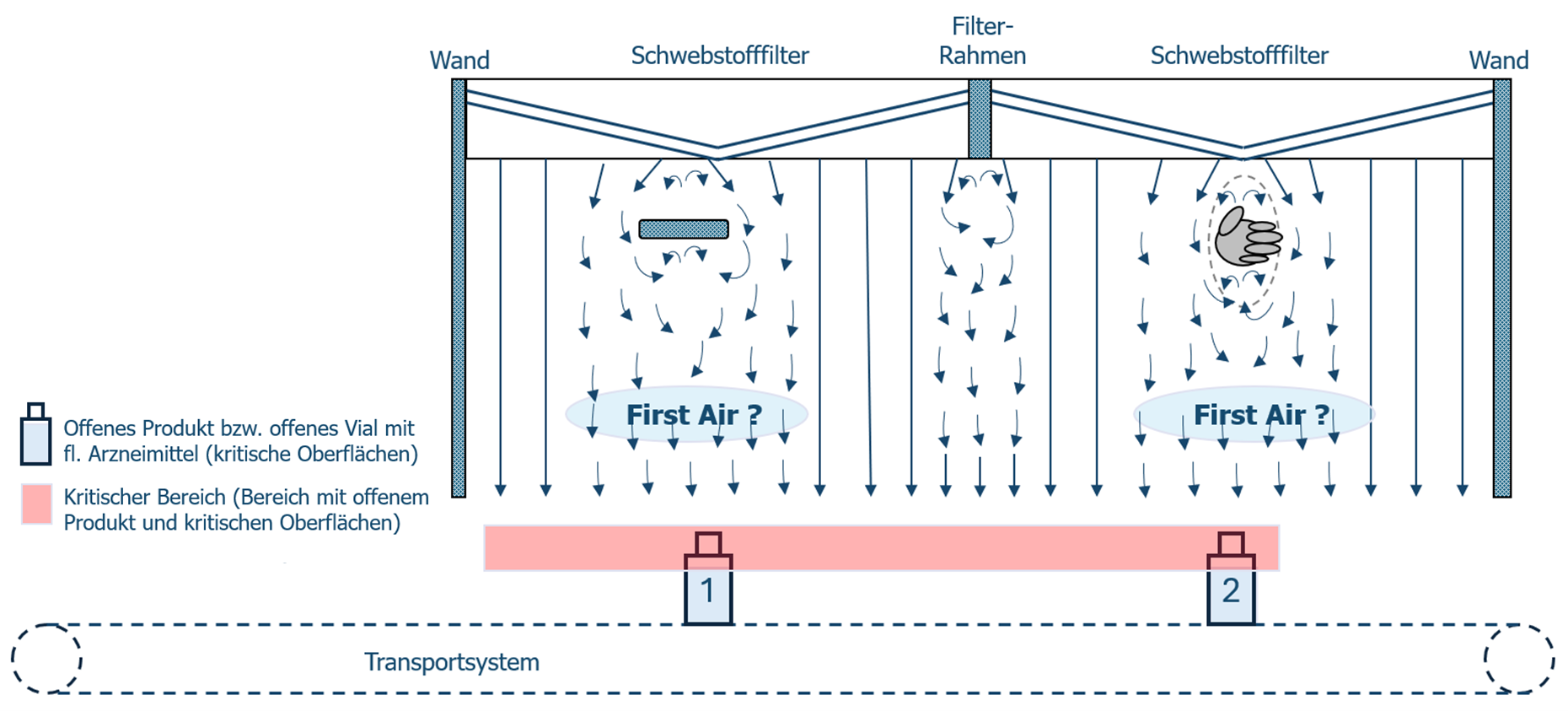
Abbildung 1 | Schematische Darstellung eines Beispiels zum First Air-Prinzip
Filterrahmen:
Der Filterrahmen ist nicht luftdurchströmt, wodurch es hier unterhalb zwangsläufig zu Verwirbelungen kommt. Die Luft strömt weiterhin von oben nach unten und zeigt somit auch die Verdrängungswirkung. Es gelangen keine Kontaminationen in diesen Luftstrom, bevor der kritische Bereich erreicht wird. Somit handelt es sich hierbei weiterhin um Erstluft (First Air), welche den rot markierten, kritischen Bereich umströmt und somit schützt.
Strömungshindernis:
Luft (First Air) aus dem Filter verwirbelt sich nach dem Strömungshindernis und gelangt in den kritischen Bereich. Falls die Oberfläche des Hindernisses sterilisiert ist, in Produktion nicht kontaminiert wird und keine Kontaminanten (Partikel, Keime) in das Wirbelgebiet eindringen können, handelt es sich trotzdem um First Air. Ist die Oberfläche „nur“ dekontaminiert (H₂O₂) ist eine Bewertung (CCS) erforderlich, ob es sich um eine potentielle Kontaminationsquelle handelt oder nicht.
Handschuh:
Bei einem Handschuh muss trotz Dekontamination mit H₂O₂ davon ausgegangen werden, dass es sich um eine Kontaminationsquelle handelt, da Handschuhe während der Produktion kontaminiert oder beschädigt werden können. Das heißt, es darf keine Luft, die den Handschuh berührt hat in den kritischen Bereich gelangen, da es sich hierbei nicht mehr um First Air handelt.
Fazit
- First Air ist definitionsgemäß die Partikel- und Keimfreie Luft, die aus dem Schwebstofffilter abströmt. Auch bei dieser Betrachtung bleibt ein minimales Restrisiko, da Filter nur zu ca. 99,99% keine Partikel durchlassen und Filtermaterial/Filterrahmen keine sterilen Oberflächen sind.
- Ziel einer First Air - Analyse ist es, das Risiko bei der Herstellung steriler Produkte (Klasse A – Bereiche) so gut wie möglich zu minimieren.
- Bei Handschuhen in RABS oder Isolatoren, muss trotz Dekontamination mit H2O2 davon ausgegangen werden, dass es sich um eine Kontaminationsquelle handelt, da Handschuhe während der Produktion kontaminiert oder beschädigt werden können -> keine First Air nach dem Handschuh, d.h. es darf keine Luft, die den Handschuh berührt hat in den kritischen Bereich gelangen.
- Zudem stellt ein Handschuh ein Strömungshindernis dar und es muss bewertet werden, ob bei einem Eingriff sich Kontaminanten abströmseitig vom Handschuh anreichern und in den kritischen Bereich gelangen können.
- Strömungshindernisse zwischen Luftfilter und kritischem Bereich (Zone mit offenem Produkt oder kritischen Oberflächen) können nicht vollständig verhindert werden. Es ist Aufgabe der CCS, jedes einzelne Strömungshindernis bezüglich des Kontaminationsrisikos zu bewerten und entsprechende Präventions- und Überwachungsmaßnahmen dafür festzulegen. Insbesondere auch bei Bestandsanlagen müssen unvermeidbare Handschuheingriffe mit Einfluss auf den kritischen Bereich in dieser Weise analysiert und bewertet werden.
- Die First Air Analyse sollte bereits im Design erfolgen. Dabei können mittels Strömungssimulation (CFD) kritische Verwirbelungen festgestellt und durch Optimierung möglichst verhindert werden.
[1] GMP-Verlag, Deutsche Übersetzung des Annex 1
Autor*innen
Michael Kuhn und Benjamin Pfändler
Leiter, STZ EURO (Steinbeis-Transferzentrum Energie-, Umwelt- und Reinraumtechnik)
E-Mail: mail@stz-euro.de
Haben Sie Fragen oder Anregungen? Bitte kontaktieren Sie uns.redaktion@gmp-verlag.de













