
Mikrobiologisches Monitoring - Keimidentifizierung
Auszug aus dem GMP-BERATER, Kapitel 10.E, Mikrobiologisches Monitoring
5 Min. Lesezeit | von Michael Rieth
Erschienen im LOGFILE 09/2026
Spätestens bei der Überschreitung des Aktionslevels im Rahmen des mikrobiologischen Monitorings sollten die nachgewiesenen Mikroorganismen identifiziert werden. Die Identifizierung liefert häufig entscheidende Hinweise auf deren Herkunft. Konventionelle Methoden stoßen dabei jedoch oft an ihre Grenzen und ermöglichen keine eindeutige Bestimmung. Erst auf der Ebene der Spezies lassen sich belastbare Rückschlüsse auf mögliche Kontaminationsquellen und die Herkunft der Mikroorganismen ziehen.
Keimidentifizierung
Im Rahmen des mikrobiologischen Monitorings sollten aufgefundene Keime zumindest bei Grenzwertüberschreitungen identifiziert werden. Man erhofft sich aus der Identifizierung Hinweise auf die Herkunft zu erhalten. Leider reichen in aller Regel konventionelle Methoden zur Keimidentifizierung nicht aus, um eindeutige Kontaminationszusammenhänge zu erkennen. Darauf wird in den Hinweisen zur Anwendung der Prüfung auf Sterilität der Ph. Eur. (Kapitel 5.1.9) ausdrücklich hingewiesen. Auch die FDA Aseptic Guidance enthält einen entsprechenden Hinweis.
Da aber die meisten mikrobiologischen Laboratorien nicht über die Möglichkeit zur molekularen Typisierung von Isolaten verfügen, muss man die vorhandenen konventionellen Methoden verwenden. Aber auch mit diesen Ergebnissen kann man auf Grund der Spezies gewisse Rückschlüsse auf die mögliche Herkunft der Mikroorganismen ziehen.
Bei Umgebungskontrollen muss man mit einem sehr unterschiedlichen Anteil der verschiedenen Gruppen von Mikroorganismen rechnen. Zudem können diese Anteile je nach untersuchtem Bereich und Jahreszeit variieren:
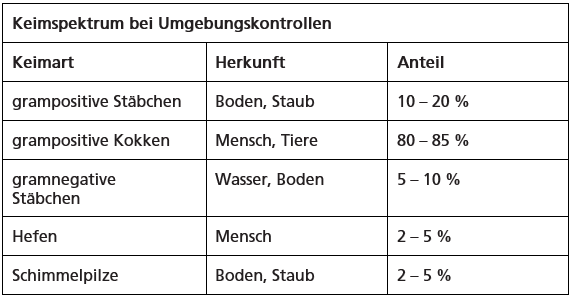
Im Folgenden soll eine Möglichkeit des Untersuchungsgangs zur Identifizierung von Isolaten (Bakterien) aus Umgebungskontrollen dargestellt werden. Ganz wichtig ist der Hinweis, dass solche Arbeiten unter das Infektionsschutzgesetz fallen und deshalb der zuständigen Behörde (Seuchenreferat des zuständigen Regierungspräsidiums oder des Gesundheitsamtes) angezeigt und von dieser genehmigt werden müssen.
Normalerweise wird man nicht alle Kolonien einer Grenzwertüberschreitung identifizieren, sondern die morphologisch unterschiedlichen Kolonien identifizieren. Außerordentlich wichtig ist, vor der Identifizierung mindestens eine, häufig sogar zwei Passagen, auf Blutagar anzulegen, um zur Einzelkolonie zu gelangen. Dadurch werden die Keime revitalisiert und erlangen die Möglichkeit, die für sie typischen biochemischen Reaktionen durchzuführen. Diese Kultur sollte im fraktionierten Ausstrich erfolgen, um möglichst mit Reinkulturen weiterzuarbeiten. Man prüft zunächst die einzelnen Kolonien (Farbe, Größe, Form, Hämolyse, eventuell Geruch, metallischer Glanz usw.) und protokolliert das Ergebnis. Mit einem Grampräparat legt man dann das weitere Vorgehen fest (Abbildung 1) 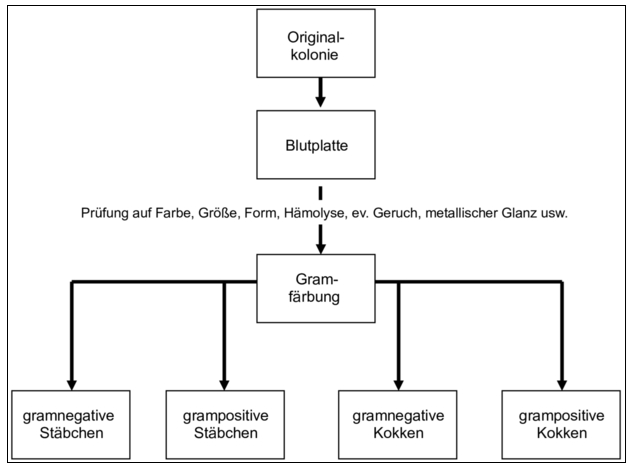
Abbildung 1 | Untersuchungsgang zur Identifizierung von Isolaten aus Umgebungskontrollen: Anzucht von Reinkulturen und Gramfärbung
In den folgenden Abbildungen finden sich die Untersuchungsgänge für
- gramnegative Stäbchen (Abbildung 2),
- grampositive Stäbchen (Abbildung 3),
- gramnegative Kokken (Abbildung 4) und
- grampositive Kokken (Abbildung 5).
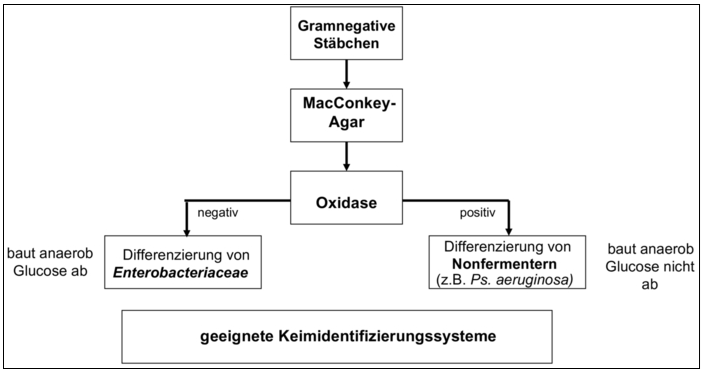
Abbildung 2 | Untersuchungsgang zur Identifizierung von Isolaten aus Umgebungskontrollen – Identifizierung von gramnegativen Stäbchen
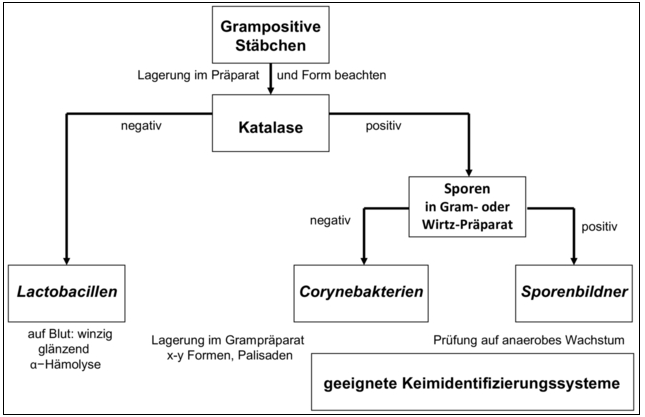
Abbildung 3 | Untersuchungsgang zur Identifizierung von Isolaten aus Umgebungskontrollen – Identifizierung von grampositiven Stäbchen
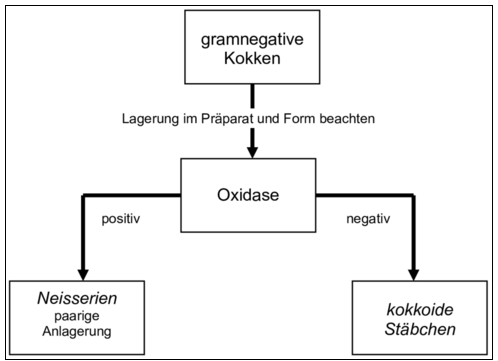
Abbildung 4 | Untersuchungsgang zur Identifizierung von Isolaten aus Umgebungskontrollen – Identifizierung von gramnegativen Kokken
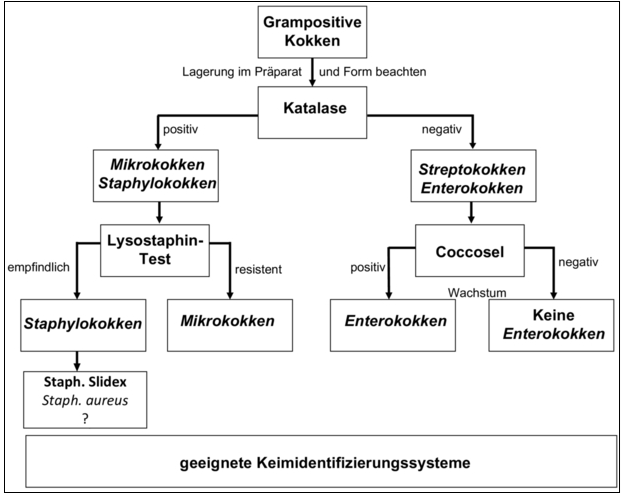
Abbildung 5 | Untersuchungsgang zur Identifizierung von Isolaten aus Umgebungskontrollen – Identifizierung von grampositiven Kokken
Es reicht nicht aus, sich nur mit Bakterien zu beschäftigen. Treten Probleme mit Pilzen auf, sollte man zunächst zwischen Hefen und Schimmelpilzen unterscheiden. Ist eine weitergehende Identifizierung erforderlich, wird man sich in aller Regel an Spezialisten (Mykologen) wenden müssen, da zumindest für Schimmelpilze keine zuverlässigen Identifizierungssysteme am Markt sind.
Da man aus Kapazitätsgründen in aller Regel nicht jeden gefundenen Mikroorganismus identifizieren kann, muss man sich überlegen, wann man die gefundenen Organismen identifizieren will und bis zu welcher Tiefe. Nach den Vorstellungen der FDA Aseptic Guidance sollte man nach Möglichkeit bis Spezies identifizieren beziehungsweise – falls angemessen – bis Genus. Bei der Entscheidung ist auch die betroffene Reinheitsklasse zu berücksichtigen.
Bei Überschreitungen des Aktionslevels in Reinheitsklasse A und B sollte man immer möglichst bis Spezies identifizieren; bei Überschreitungen des Warnlevels reicht in den meisten Fällen die Identifizierung bis zum Genus. Bei Verdacht auf spezielle Mikroorganismen, z. B. Endosporenbildner oder Pseudomonaden, sollte man diese ebenfalls identifizieren.
In Reinheitsklasse C reicht bei Überschreitungen des Aktionslevels in der Regel eine Identifizierung bis zum Genus. Bei Verdacht auf spezielle Mikroorganismen, z. B. Endosporenbildner oder Pseudomonaden, sollte man auch hier diese Bakterien identifizieren.
Bei Isolaten aus der Reinraumklasse D, E und F sollte man besonders häufig auftretende Kolonien identifizieren. In vielen Fällen wird bereits eine Gramfärbung ausreichen. Hierbei kann man häufig bereits kritische Mikroorganismen, wie gramnegative Stäbchen und Endosporenbildner erkennen.
Interessant ist auch ein Vorschlag (Entscheidungsbaum) aus der Laborpraxis: Bei grampositiven Kokken stellt man zunächst fest, ob es sich um Staphylococcus aureus handelt. Ist dies der Fall, dann versucht man die Ursache zu finden, um die Quelle zu eliminieren. Anderenfalls berichtet man nur „Grampositive Kokken“. Bei Hefen und Schimmelpilzen führt man eine Identifizierung nur durch, wenn diese Organismen öfter auftreten. Anderenfalls berichtet man nur „Hefen oder Schimmelpilze“.
Haben Sie Fragen oder Anregungen? Bitte kontaktieren Sie uns.redaktion@gmp-verlag.de











