
Kalibrierung der Messstellen bei Pharmawassersystemen
Auszug aus dem GMP-BERATER, Kapitel 5.E.10, Kalibrierung
7 Min. Lesezeit | von Fritz Röder
Erschienen im LOGFILE Leitartikel 35/2022
Die Kalibrierung der Messstellen ist von enormer Bedeutung, denn nur mit richtigen Werten kann der Zustand der Anlage korrekt interpretiert werden. Die Kalibrierung ist auch eine grundsätzliche Vorgabe aus dem EU-GMP-Leitfaden (Punkt 3.41 EU-GMP-Leitfaden). Deshalb ist es unbedingt notwendig, die Kalibrierung von qualitätsrelevanten Messeinrichtungen genauso regelmäßig durchzuführen wie Wartungen.
Die Festlegung, welche Messeinrichtungen zu kalibrieren sind (kritische Messeinrichtungen), sollte über eine Risikoanalyse erfolgen und eine Einteilung in verschiedene Risikoklassen beinhalten. Eine solche Einteilung hat den Vorteil, dass die Begründung zur Festlegung des Kalibrierintervalls eine Rationale hat. Zusätzlich existiert bei Wassersystemen die Besonderheit, dass manche Online-Sensorik (z. B. TOC, Leitfähigkeit) eventuell für die Freigabe des Wassers als Inhaltsstoff verwendet wird – hier wird das „PAT-Konzept“ gelebt. Ist dies der Fall, haben die Daten dieser Sensoren eine besondere Kritikalität und werden durch den Leiter der Qualitätskontrolle genehmigt.
Bei der Risikoanalyse sollten die Messstellen nach folgenden Aspekten bewertet werden:
- kritisch für das Produkt
- kritisch für den Prozess
- kritisch für die Anlage
- kritisch für die Sicherheit
- nicht kritisch
Abbildung 1 zeigt eine mögliche Klassifizierung und Festlegung von Kalibrierintervallen auf Basis dieser Aspekte.
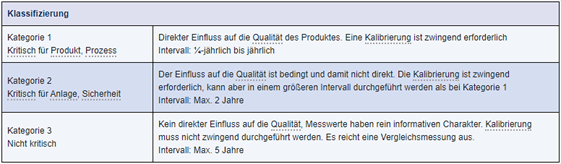
Abbildung 1 Risikoklassifizierung von Messstellen
Zusätzlich zur Kritikalität eines Parameters können auch noch weitere Argumente in die Festlegung der Messgenauigkeit und der Kalibrierfrequenz mit einbezogen werden, z. B.:
- Wie genau kann die betreffende Sensorik überhaupt ausgeführt werden?
Beispielsweise können Kräfte/Drücke sehr präzise und in Echtzeit gemessen werden. Ein TOC-Messgerät kann zwar auch sehr genau messen, allerdings bewegen sich typische Messwerte im Bereich der Bestimmungsgrenze (LOQ), wo es eben ungenauer wird. Zudem liefert ein TOC-Messgerät aufgrund seiner Methodik ca. alle 5-10 Minuten einen Messwert. - Wie stabil läuft der Wasseraufbereitungsprozess? Wie stark schwankt er? Welche Erfahrungen liegen bereits damit vor?
- Gibt es weitere Messeinrichtungen, die supportive Daten liefern und bei einem Ausfall der primären Messung ersatzweise herangezogen werden könnten?
Eine Übersicht über alle Messeinrichtungen, unabhängig von der Kategorie, muss vorhanden sein. Dies ist ein wesentlicher Punkt innerhalb einer Inspektion. Die Kalibrierungen der Messstellen müssen in das Wartungssystem aufgenommen werden und dort nach dem gleichen Vorgehen wie ein Wartungsvorgang bearbeitet und dokumentiert werden. Abbildung 2 zeigt die Zuordnung relevanter Messstellen eines Wassersystems zu den vorgenannten Kategorien unter gleichzeitiger Angabe der Kalibrierintervalle.
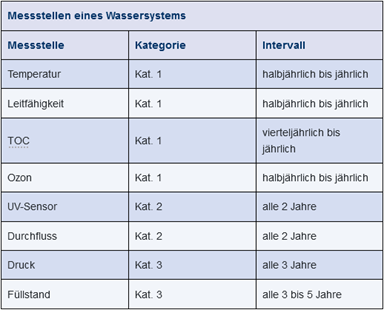

Abbildung 2 Klassifizierung und Kalibrierintervalle relevanter Messstellen
Es wird darauf hingewiesen, dass ein TOC-Messgerät zusätzlich zur Kalibrierung einem System Suitability Test unterzogen wird.
Für die Kalibrierung müssen folgende Punkte festgelegt und im Rahmen gelenkter Dokumente beschrieben sein:
- Kalibrierfrequenzen mit Abweichungen
- Identifizierungscode der Messstelle
- Kalibrierungsbereich
- Kalibriergenauigkeit
- Anzahl der Kalibrierpunkte
- Kalibriervorschrift
- Ggf. Justagegrenzen, wenn vorhanden
Die Prüfmittel müssen ausreichend genau sein (Richtwerte 3 bis 10 mal genauer als die eingesetzten Messinstrumente).
Festgestellte Abweichungen bei der Kalibrierung müssen im Abweichungsmanagement des QS-Systems vom Betreiber bearbeitet werden. Wichtig bei einer Abweichung dieser Art ist die Risikobewertung bezogen auf die Produktqualität.
Haben Sie Fragen oder Anregungen? Bitte schreiben Sie uns: redaktion@gmp-verlag.de











