
SOPs schreiben war noch nie so einfach!
Sonderausgabe zum Relaunch der SOP-Sammlung für die Pharmaindustrie
5 Min. Lesezeit | von Dr. Doris Borchert
Erschienen im LOGFILE Special Oktober 2024
SOPs braucht jedes Pharmazeutische Unternehmen. Und jedes Unternehmen braucht – neben individuell unterschiedlichen Arbeitsanweisungen – die gleichen „Standard-SOPs“.
Das sind z. B. die Elemente des Pharmazeutischen Qualitätssystems wie Änderungs- und Abweichungsmanagement, CAPA und PQR oder Reklamationen und Rückruf. Auch Abläufe rund um das Thema Datenintegrität und Dokumentation müssen in jedem Betrieb beschrieben werden. Hinzu kommen alle Qualifizierungs- und Validierungsprozesse – die Liste ließe sich beliebig verlängern.
All diesen Prozessen ist eines gemeinsam: es gibt regulatorische Anforderungen (WAS muss ich tun?), für deren Umsetzung (WIE soll ich es machen?) jeder selbst verantwortlich ist.
Als SOP-Autor*in wissen Sie, welchen Arbeitsaufwand der Abgleich der betriebsinternen Abläufe mit den regulatorischen Anforderungen bedeutet. Dabei gibt es Abläufe und Vorgänge, die in vielen pharmazeutischen Unternehmen ähnlich gehandhabt werden könnten.
Warum also das Rad jedes Mal neu erfinden?
Die SOP-Sammlung für die Pharmaindustrie enthält über 50 Beispiel-SOPs für die wichtigsten Themen. Mit diesen Vorlagen möchten wir Ihnen die Arbeit bei der Erstellung oder Überarbeitung von SOPs erleichtern.
Themengebiete der SOP-Sammlung:
- Qualitätsmanagement
- Qualitätskontrolle
- Personal
- Dokumentation
- Gebäude und Anlagen
- Material und Produkt
- Transport

Diese Vorteile bietet Ihnen die SOP-Sammlung:
Das Konzept der SOP-Sammlung ist einzigartig: es verbindet regulatorische Anforderungen mit praxistauglichen Umsetzungsvorschlägen im Rahmen einer fiktiven Firma.
- Die aktuellen regulatorischen Anforderungen werden umgesetzt.
- Die Inhalte der SOPs werden geschlossen dargestellt und kommentiert.
- Die SOPs sind aufeinander abgestimmt.
- Die Grundlage bildet ein Site Master File.
- Stellenbeschreibungen und Organigramm ergänzen die Sammlung.
Die SOP-Sammlung wird fortlaufend durch neue SOPs ergänzt. Bestehende SOPs werden aktualisiert, um den aktuellen GMP-Anforderungen zu entsprechen.
Jetzt neu: Die SOP-Sammlung als Online-Portal!
Zu ihrem 15-jährigen Bestehen präsentiert sich die SOP-Sammlung im neuen Gewand: ein benutzerfreundliches Online-Portal mit vielen Zusatzfunktionen macht das Arbeiten mit der SOP-Sammlung jetzt noch leichter.
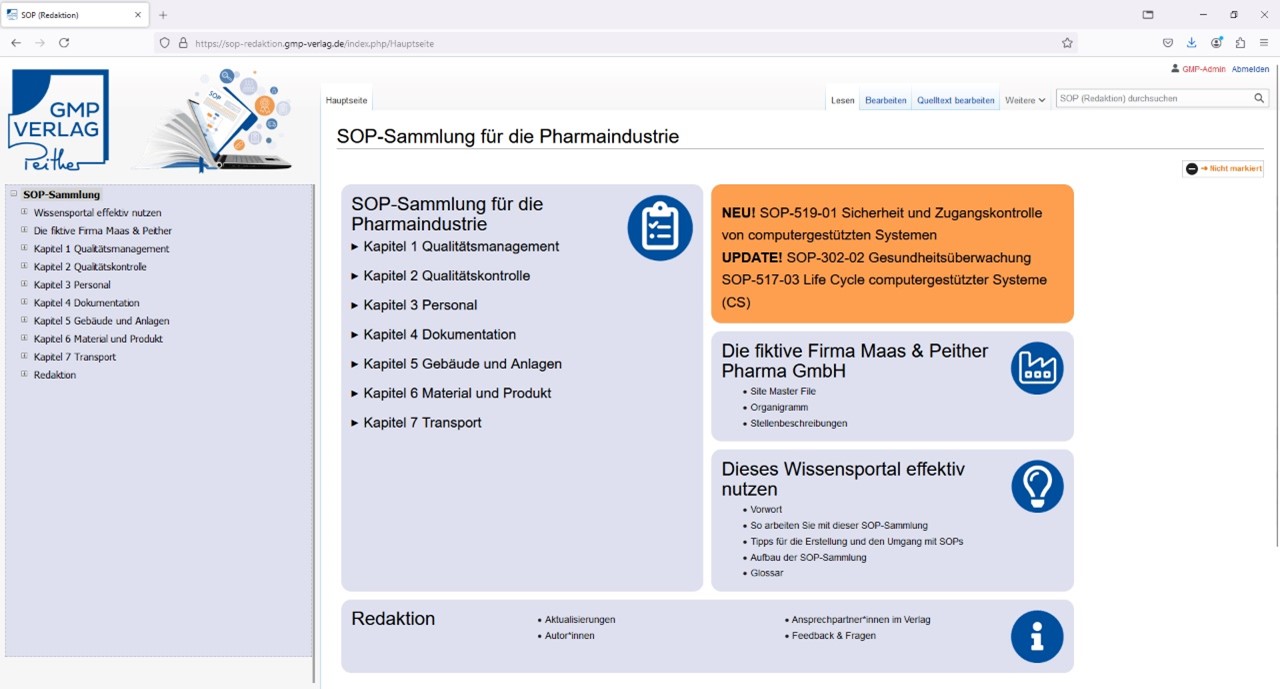
Die Startseite vermittelt einen Überblick über die einzelnen Bereiche der SOP-Sammlung. Neben den 7 Themengebieten finden Sie hier auch die Beschreibung der fiktiven Firma Maas&Peither Pharma GmbH, Informationen zu neuen und aktualisierten Inhalten sowie Tipps und Tricks zur Nutzung des Portals.
Die einzelnen SOPs können im Navigationsbaum aufgerufen werden. Auf der Startseite finden Sie die Worddateien zum Herunterladen und gelangen direkt zu den Kapiteln der SOP.
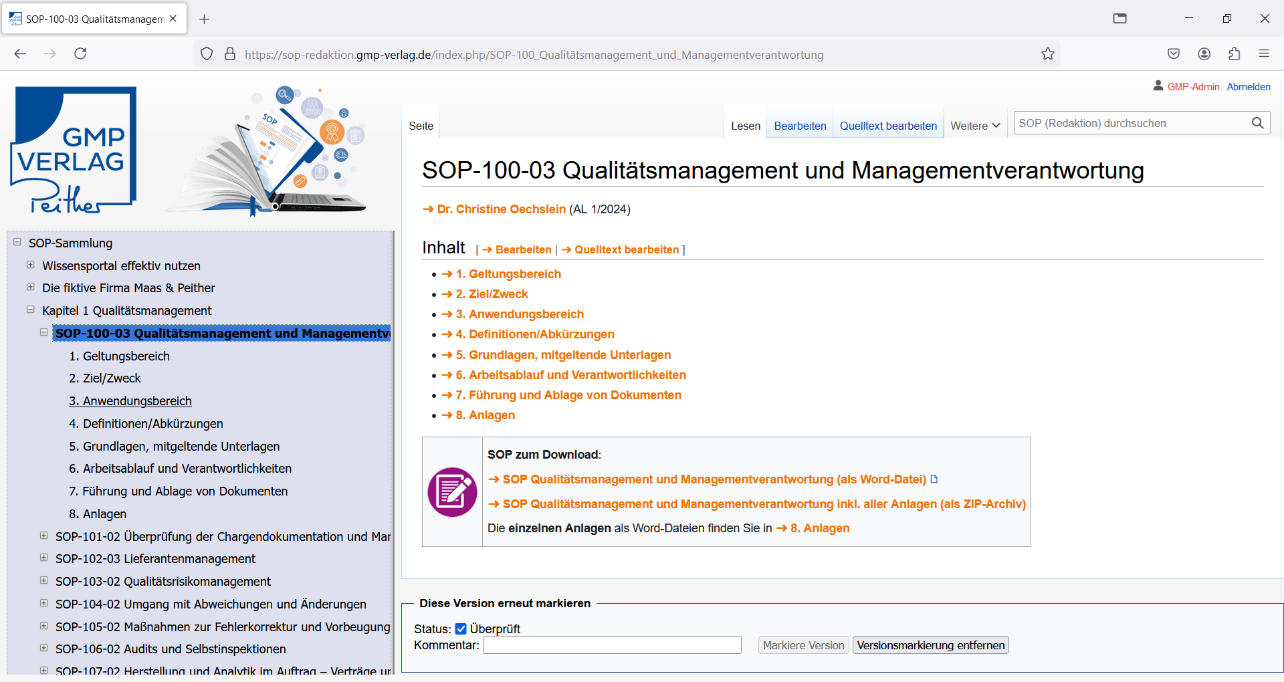
Jede SOP besteht aus dem Kerndokument (Durchführung, Verantwortlichkeiten etc.) und wertvollen Anlagen (z. B. Ablaufdiagramm, Formblätter, Checklisten u.ä.).
Die SOP-Sammlung sichert einen reibungslosen Ablauf Ihrer GMP-Prozesse!
Möchten Sie mehr erfahren? Dann fordern Sie kostenlos und unverbindlich Ihren Demo-Zugang an!
Haben Sie Fragen oder Anregungen? Bitte schreiben Sie uns: redaktion@gmp-verlag.de












