
Prozessintegriertes Containment
Auszug aus dem GMP-Fachwissen Planung von pharmazeutischen Produktionsanlagen
6 Min. Lesezeit | von Richard Denk
Erschienen im LOGFILE Leitartikel 07/2022
Zur Reduzierung von Containment-Transferschritten kann das Containment auch in den Prozess integriert werden. Wie dies durchgeführt werden kann, wird anhand eines Beispiels an einem Wirbelschichter beschrieben.
Ein prozessintegriertes Containment (Prozesshülle) wäre ein wesentlicher Fortschritt bei der Herstellung von hochaktiven/hochgefährlichen Substanzen. Anstatt Containment-Transfersysteme zu verwenden, um die pharmazeutischen Substanzen von einem Prozess-System zum nächsten zu überführen, könnte das Containment in den Prozess integriert werden.
Die nachfolgenden Abbildungen zeigen schematisch den Einsatz einer Prozesshülle in einem Wirbelschichter. Derartige Systeme werden in der kommerziellen Arzneimittelherstellung bisher nicht eingesetzt. Mit ihrer Hilfe könnten aber Herausforderungen, die mit der Reinigung sowie mit einem möglichen Containment-Bruch beim Befüllen oder Entleeren von Wirbelschichtanlagen verbundenen sind, deutlich reduziert werden.
Der Prozessapparat erfüllt in diesem Fall die Funktion der zweiten Schutzhülle des Containments und beinhaltet alle notwendigen Ansteuerungen. Das prozessintegrierte Containment (Prozesshülle) wird in den Prozessapparat eingesetzt, wie in Abbildung 4.I-58 bis Abbildung 4.I-60 gezeigt wird. Dieses prozessintegrierte Containment kann entweder aus einem Einwegmaterial oder aus einem Edelstahlbehälter bestehen. In beiden Fällen kommt das pharmazeutische Produkt nicht mit dem Prozessapparat in direkten Kontakt, sondern wird innerhalb des prozessintegrierten Containments (Prozesshülle) verarbeitet. Nach dem Prozessende wird das integrierte Containment (Prozesshülle) aus dem Prozessapparat entnommen. Ein wesentlicher Vorteil besteht darin, dass der Prozessapparat nicht kontaminiert wird, so dass dieser sofort wieder für die nächste Integration eines prozessintegrierten Containment (Prozesshülle) verwendet werden kann.
Auch kann der Prozessapparat als zusätzlicher Reinraum fungieren, wodurch das Raumdesign außerhalb des Prozessapparats reduziert werden kann. So können Luftwechselraten und die Konditionierung der Reinraumluft auf ein kleinstmögliches Maß reduziert und die Umwelt deutlich entlastet werden.
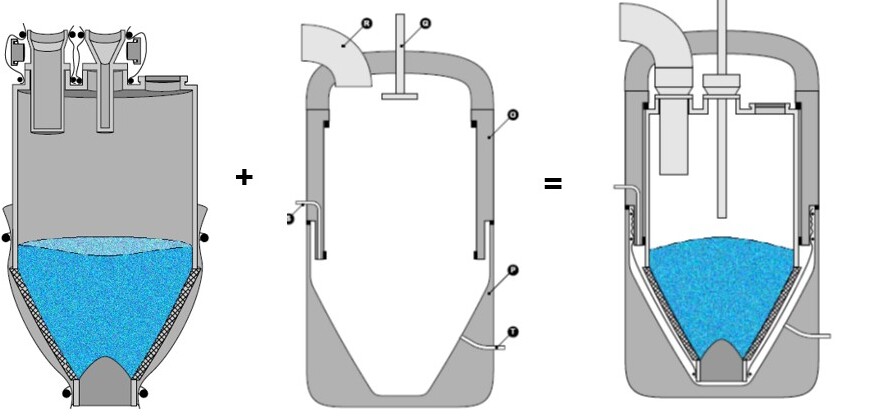
Abbildung 4.I-58 Mit Produkt gefüllte Prozesshülle (links) wird in den Prozessbehälter (Mitte) eingesetzt (Quelle: Richard Denk)

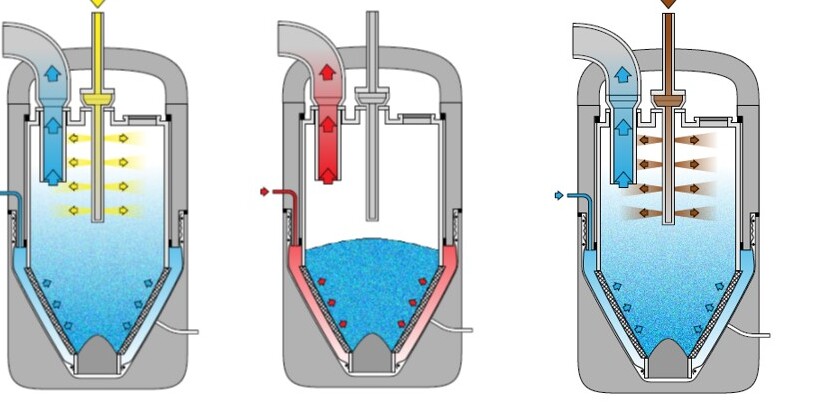
Abbildung 4.I-59 Prozessabläufe innerhalb des Prozessbehälters:links: Granulation, Mitte: Trocknung, rechts: Beschichtung (Quelle: Richard Denk)

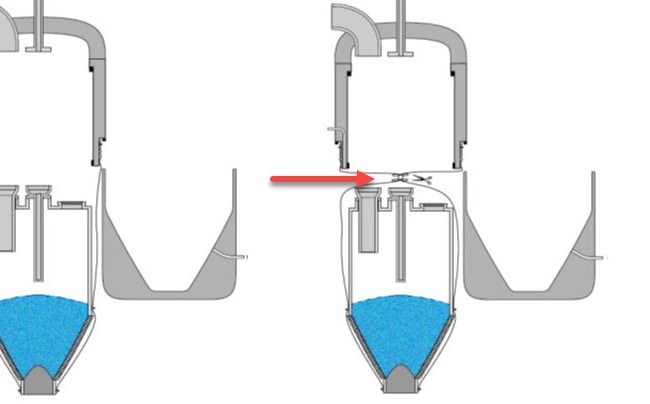
Abbildung 4.I-60 Auswechseln der Prozesshülle aus dem Prozessbehälter (Quelle: Richard Denk)
Das prozessintegrierte Containment bietet folgende Vorteile:
- Der Prozessapparat wird durch das hochaktive/hochgefährliche pharmazeutische Produkt nicht kontaminiert.
- Die Reinigung des Prozessapparates ist nicht nötig.
- Der Prozessapparat kann als sekundäres Containment wirken. Somit können die Reinraumanforderungen außerhalb des Prozessapparates deutlich reduziert werden.
- Erhebliche Kosten- und Energie-Einsparungen durch reduzierten Aufwand für Luftwechsel, Konditionierung der Luft, Monitoring des Raumes sowie der Reinigung des Raumes.
- Schneller Produktwechsel, da die Prozesshülle komplett aus dem Prozessapparat entfernt wird.
- Die Prozesshülle kann aus einem Einweg- oder Mehrwegbehältnis hergestellt werden.
- Mögliche Oberflächenbeschädigungen, die Auswirkungen auf die Reinigung haben, befinden sich nicht mehr in dem Prozess sondern in der Prozesshülle, wo diese einfach ausgebessert werden können.
Haben Sie Fragen oder Anregungen? Bitte schreiben Sie uns: redaktion@gmp-verlag.de











